|
||||
|
Глава 5 Атомы [35] Закон Пруста Успех Лавуазье показал химикам, что применение количественных измерений может помочь понять суть химических реакций. Метод количественных измерений был использован, в частности, при исследовании кислот. Кислоты образуют естественную группу веществ, обладающих рядом характерных свойств. Они химически активны, реагируют с такими металлами, как цинк, олово или железо, которые при растворении в кислотах выделяют водород. Кислоты имеют кислый вкус, вызывают характерные изменения цветов некоторых красителей и т. д. Кислотам противостоит группа веществ, называемых основаниями. (Сильные основания получили название щелочей.) Эти вещества имеют горький вкус, химически активны, меняют цвета красителей, но на противоположные по сравнению с кислотами и т. д. Растворы кислот нейтрализуют растворы оснований. Другими словами, смесь кислоты и основания, взятых в определенном соотношении, не проявляет свойств ни кислоты, ни основания. Эта смесь представляет собой раствор соли, которая обычно химически значительно менее активна, чем кислота или основание. Таким образом, при смешении соответствующих количеств растворов сильной и едкой кислоты (соляной кислоты) с сильной и едкой щелочью (гидроксидом натрия) получается раствор хлорида натрия, т. е. обыкновенной поваренной соли. Реакции нейтрализации заинтересовали немецкого химика Иеремию Веньямина Рихтера (1762—1807). Начав их изучение, он измерил точные количества различных кислот, необходимых для нейтрализации определенных количеств того или иного основания, и наоборот. Результаты измерений показали, что, проводя реакцию нейтрализации, нельзя пользоваться приемами повара, который в соответствии со своим вкусом может увеличить или уменьшить количество того или иного компонента; в данном случае необходимы определенные и постоянные количества веществ. Рихтер изложил свои взгляды в книге «Стехиометрия, или искусство измерения химических элементов», которая вышла в трех частях в 1792—1794 гг. [36] Основываясь на результатах многочисленных анализов солей, Рихтер составил ряд нейтрализации, который показывал относительные весовые количества кислот и щелочей, необходимых для нейтрализации. Здесь речь шла об эквивалентном (соединительном) весе — постоянном весе одного химического вещества, реагирующего с другим веществом, также имеющим постоянный вес. Таким образом, Рихтеру принадлежит формулировка закона эквивалентов. Вскоре после опубликования работ И. Рихтера два французских химика вступили в яростный спор о том, присуща ли такая определенность только реакциям кислотно-основной нейтрализации или химическим процессам вообще. В принципе вопрос стоял так: если какое-либо соединение состоит из двух (трех или четырех) элементов, всегда ли соотношение этих двух элементов постоянно? Меняются ли эти соотношения в зависимости от способа получения соединения? Одним из споривших химиков был К. Л. Бертолле, который, как мы упоминали выше, совместно с Лавуазье разработал современную химическую терминологию (см. гл. 4). Бертолле придерживался второй точки зрения и считал, что соединение, состоящее из элементов x и y, содержит большее количество x, если при получении этого соединения использовался большой избыток x. Французский химик Жозеф Луи Пруст (1754—1826), который работал в Испании, придерживался противоположного мнения. С помощью тщательных анализов Пруст в 1799 г. показал, например, что карбонат меди характеризуется определенным весовым соотношением меди, углерода и кислорода вне зависимости от того, каким способом эта соль получена в лаборатории или каким способом выделена из природных источников. Соединение всегда содержит 5.3 части меди, 4 части кислорода и 1 часть углерода. Более того, Пруст установил, что постоянство соотношений компонентов наблюдается и в ряде других соединений. Он сформулировал общее правило, согласно которому все соединения содержат элементы в строго определенных пропорциях (а не в любых сочетаниях) вне зависимости от условий получения этих соединений. Это правило называется законом постоянства состава, или иногда законом Пруста. (Пруст также показал, что Бертолле, пытаясь доказать, что состав определенных соединений меняется в зависимости от метода их получения, пришел к ошибочным выводам из-за неточности анализов и использования недостаточно чистых исходных соединений.) В первые годы девятнадцатого столетия стало совершенно очевидно, что Пруст прав. Закон постоянства состава был уточнен и стал краеугольным камнем химии [37]. И тем не менее с момента открытия закона Пруста существовали серьезные сомнения в его справедливости. В конце концов, почему закон постоянства состава всегда должен быть справедлив? Почему какое-то соединение всегда должно содержать 4 части x и 1 часть y, и почему оно не может содержать, например, 4.1 или 3.9 части x и 1 часть y? Если допустить, что материя является сплошной (а не дискретной), то понять это трудно. Почему элементы не могут смешиваться в несколько иных пропорциях? А как будет обстоять дело, если материя дискретна — состоит из атомов? Предположим, соединение образуется в результате связывания одного атома x с другим атомом y и никак иначе. (Такая комбинация атомов впоследствии получила название «молекула» от латинского moles — небольшая масса.) Если предположить, что вес атома x в 4 раза больше, чем вес атома y, то в этом случае соединение содержит точно 4 части x и 1 часть y. Чтобы это соотношение изменилось, атом у должен соединиться с таким количеством x, которое чуть больше или чуть меньше одного атома x. Поскольку еще со времен Демокрита атом считался неделимой частицей материи, было нелогично предполагать, что от него можно «отколоть маленький кусочек» или что к нему можно присоединить малую долю второго атома. Другими словами, если признать атомное строение материи, то из этого положения закон постоянства состава вытекает как естественное следствие. Более того, поскольку справедливость закона постоянства состава — неоспоримый факт, то, следовательно, атомы действительно являются неделимыми частицами. Теория Дальтона [38] Английский химик Джон Дальтон (1766—1844), который вошел в историю химии как первооткрыватель закона кратных отношений и создатель основ атомной теории, прошел через всю цепь этих размышлений. Основные положения теории Дальтон вывел из сделанного им самим открытия. Он обнаружил, что два элемента могут соединяться друг с другом в различных соотношениях, но при этом каждая новая комбинация элементов представляет собой новое соединение (рис. 9). Так, например, при образовании углекислого газа 3 части углерода (по весу) соединяются с 8 частями кислорода, а 3 части углерода и 4 части кислорода дают угарный газ (моноксид углерода). Соотношение количеств кислорода, содержащегося в этих соединениях, представляет собой соотношение малых целых чисел. Восемь частей кислорода дают углекислый газ, 4 части кислорода — угарный (оксид углерода), т. е. в первом соединении кислорода вдвое больше. В 1803 г. Дальтон обобщил результаты своих наблюдений и сформулировал важнейший закон химии — закон кратных отношений. Этот закон полностью отвечает атомистическим представлениям. Предположим, например, что атомы кислорода в 3 раза тяжелее атомов углерода. Если монооксид углерода образуется в результате сочетания одного атома углерода с одним атомом кислорода, то в этом соединении соотношение весовых частей углерода и кислорода должно быть равно 3:4. В диоксиде же углерода, состоящем из одного атома углерода и двух атомов кислорода, оно должно быть 3:8. Поскольку было найдено, что элементы соединяются в кратных отношениях, следовательно, соединения различаются по составу на целые атомы. Разумеется, предполагаемые различия в составе и закон кратных отношений справедливы лишь при условии, что материя действительно состоит из крошечных неделимых атомов. Выдвигая новую версию атомистической теории, опиравшуюся на законы постоянства состава и кратных отношений, Дальтон как дань уважения Демокриту сохранил термин «атом» и назвал так считавшиеся в то время неделимыми мельчайшие частицы, составляющие материю. В 1808 г. он опубликовал труд «Новая система химической философии», в которой изложил атомистическую теорию уже более подробно. В том же году справедливость закона кратных отношений была подтверждена исследованиями другого английского химика — Уильяма Гайда Уолластона (1766—1828). Уолластон всячески способствовал утверждению атомистической теории, и взгляды Дальтона со временем завоевали всеобщее признание. Атомистическая теория нанесла последний удар по бытовавшим еще представлениям о возможностях взаимных переходов элементов-стихий. Стало очевидным, что различные металлы состоят из атомов различных видов, и, поскольку атомы считались в то время неделимыми и незаменяемыми (см., однако, гипотезу Праута), бесполезно было надеяться, что когда-нибудь удастся атом свинца превратить в атом золота [39]. О непосредственном наблюдении атомов Дальтона, даже под микроскопом, не могло быть и речи: для этого они слишком малы. Однако с помощью косвенных измерений можно получить представление об их относительном весе. Например, 1 часть (по весу) водорода соединяется с 8 частями кислорода, образуя воду. Если молекула воды состоит из одного атома водорода и одного атома кислорода, то, следовательно, атом кислорода в 8 раз тяжелее атома водорода. Если условно принять, как это и делал Дальтон, вес атома водорода за 1, то вес атома кислорода при этом соответственно равен 8. Далее, если 1 часть водорода соединяется с 5 частями азота, образуя аммиак, и если молекула аммиака состоит из одного атома водорода и одного атома азота, то, следовательно, атомный вес азота должен быть равен 5. Рассуждая таким образом, Дальтон составил первую таблицу атомных весов [40]. Эта таблица, хотя, вероятно, и была самой важной работой Дальтона, в ряде аспектов оказалась совершенно ошибочной. Основное заблуждение Дальтона заключалось в следующем. Он был твердо убежден, что при образовании молекулы атомы одного элемента соединяются с атомами другого элемента попарно. Исключения из этого правила Дальтон допускал лишь в крайних случаях. Тем временем накапливались данные, свидетельствующие о том, что подобное сочетание атомов «один к одному» отнюдь не является правилом. Противоречие проявилось, в частности, при изучении воды, причем еще до того, как Дальтон сформулировал свою атомную теорию. Здесь впервые в мир химии проникло электричество. Об электричестве знали еще древние греки; было известно, что кусочек янтаря, если его потереть, способен притягивать легкие предметы. Однако лишь спустя столетия английский физик Уильям Гильберт (1540—1603) сумел показать, что такой же способностью обладает и ряд других веществ. Примерно в 1600 г. Гильберт предложил вещества такого типа называть «электриками» (от греческого ???????? — янтарь). Как выяснилось, вещество, способное после натирания или какого-либо другого воздействия притягивать к себе легкие предметы, переносит электрический заряд или содержит электричество. В 1733 г. французский химик Шарль Франсуа де Систернэ Дюфе (1698—1739) установил, что существуют два вида электрических зарядов: один из них возникает на стекле («стеклянное электричество»), а другой — на янтаре («смоляное электричество»). Вещество, несущее заряд одного вида, притягивает вещество, несущее заряд другого вида, но два одинаково заряженных вещества взаимно отталкиваются. Бенджамин Франклин (1706—1790), великий американский ученый, выдающийся государственный деятель и дипломат, в сороковых годах XVIII в. выдвинул новую гипотезу. Он предположил, что существует единый электрический флюид и что вид электрического заряда зависит от содержания этого флюида. Если содержание электрического флюида превышает некоторую норму, вещество несет заряд одного вида, если же этого флюида содержится меньше нормы, вещество несет заряд другого вида. Франклин считал, что стекло содержит электрического флюида больше нормы и поэтому несет положительный заряд. Смола же, по его мнению, несет отрицательный заряд. Термины, предложенные Франклином, используются до сих пор, хотя в них вкладывается иной смысл, так как в настоящее время представления о причинах прохождения тока противоположны тем, которые были приняты во времена Франклина. В 1800 г. итальянский физик Алессандро Вольта (1745—1827) сделал важное открытие. Он установил следующее: два куска металла (разделенные растворами, способными проводить электрический заряд) можно расположить таким образом, что по соединяющей их проволоке пойдет «ток электрических зарядов», или электрический ток. Вольта сконструировал первую электрическую батарею, представлявшую собой столб из 20 пар металлических пластинок двух разных металлов. Такая батарея, известная под названием Вольтова столба, явилась первым источником постоянного тока. Электрический ток в такой батарее образуется в результате химической реакции, в которой участвуют оба металла и разделяющий их раствор. Результаты работы Вольта явились первым несомненным доказательством того, что между химическими реакциями и электричеством существует определенная связь. Однако это предположение было полностью разработано только в следующем столетии. Если в результате химической реакции возникает электрический ток, то естественно предположить, что и электрический ток может изменять материю и вызывать химическую реакцию. И действительно, всего через шесть недель после первого описания Вольтой своей работы два английских химика — Уильям Николсон (1753—1815) и Энтони Карлайл (1768—1840) продемонстрировали наличие такой обратной зависимости. Пропустив электрический ток через воду, они обнаружили, что на электропроводящих полосках металла, опущенных в воду, появляются пузырьки газа. Как выяснилось, на одной из полосок выделяется водород, на другой — кислород. В сущности Николсон и Карлайл при помощи электрического тока разложили воду на водород и кислород. Другими словами, они впервые провели электролиз воды. Если Кавендищ соединил водород и кислород в воду, то Николсон и Карлайл осуществили обратную реакцию. Выделявшиеся по мере разложения воды водород и кислород они собирали в отдельные сосуды. Последующие измерения показали, что объем водорода вдвое превышает объем кислорода. Конечно, водород легче, чем кислород, но поскольку объем водорода был больше, следовательно, в молекуле воды атомов водорода должно быть больше, чем атомов кислорода. Объем выделившегося водорода вдвое превысил объем кислорода, поэтому вполне естественно было предположить, что каждая молекула воды содержит два атома водорода и один атом кислорода, а не по одному атому каждого элемента, как считал Дальтон. Таким образом, проведенный эксперимент подтвердил предположение о том, что одна часть водорода (по весу) соединяется с 8 частями (также по весу) кислорода. А если это предположение справедливо, то, следовательно, 1 атом кислорода в 8 раз тяжелее двух атомов водорода взятых вместе и, таким образом, в 16 раз тяжелее одного атома водорода. Если вес водорода принять за единицу, то атомный вес кислорода составит 16, а не 8. Гипотеза Авогадро [41] Результаты исследований Николсона и Карлайла были подкреплены работой французского химика Жозефа Луи Гей-Люссака (1778—1850). Гей-Люссак установил, что два объема водорода, соединяясь с одним объемом кислорода, образуют воду. Далее, он нашел, что когда газы образуют соединение, соотношение их объемов всегда представляет собой соотношение кратных чисел. В 1808 г. Гей-Люссак опубликовал сообщение об открытом им законе объемных отношений. В свете этого закона представлялось вполне допустимым, что молекула воды состоит из двух атомов водорода и одного атома кислорода. Используя этот закон, можно было также решить, наконец, сколько атомов азота и водорода в аммиаке. А после того как было установлено, что в молекуле аммиака содержится один атом азота и три (а не один) атом водорода, выяснилось, что атомная масса азота равна не примерно 5, а 14. Рассмотрим теперь водород и хлор. Эти два газа, соединяясь, образуют третий газ — хлорид водорода. При этом один объем водорода соединяется с одним объемом хлора, и вполне можно предположить, что молекула хлорида водорода состоит из одного атома водорода и одного атома хлора. Предположим теперь, что газообразный водород и газообразный хлор состоят из одиночных атомов, далеко отстоящих друг от друга, и что эти атомы соединяются попарно, образуя молекулы хлорида водорода, также далеко отстоящие друг от друга. Начнем со 100 атомов водорода и 100 атомов хлора. Эти 200 далеко отстоящих друг от друга частиц соединяются попарно и образуют 100 молекул хлорида водорода. В результате от 200 далеко отстоящих друг от друга частиц (атомов) остается только 100 также удаленных друг от друга частиц (молекул). Если пространство между ними везде одинаково, то тогда один объем водорода и один объем хлора в сумме (всего два объема) должны были бы составить только один объем хлорида водорода. Однако фактические данные говорят о том, что один объем водорода, соединяясь с одним объемом хлора, дает два объема хлорида водорода. Поскольку два объема газа, взятые для проведения опыта, остаются теми же двумя объемами после завершения опыта, то, следовательно, число частиц должно оставаться одним и тем же и до начала и после завершения опыта. Предположим далее, что газообразный водород существует не в виде отдельных атомов, а в виде молекул водорода, каждая из которых состоит из двух атомов, а газообразный хлор состоит из молекул хлора, также двухатомных. В этом случае 100 атомов водорода — это 50 далеко отстоящих друг от друга частиц водород-водород, а 100 атомов хлора — это 50 далеко отстоящих друг от друга частиц хлор-хлор, т. е. всего 100 частиц. При образовании хлорида водорода происходит перегруппировка частиц: возникает атомная комбинация водород-хлор. При этом 100 атомов водорода и 100 атомов хлора дают 100 молекул хлорида водорода (каждая из молекул содержит по одному атому каждого вида). Следовательно, 50 молекул водорода и 50 молекул хлора образуют 100 молекул хлорида водорода. Этот вывод совпадает с результатами наблюдений, которые показывают, что один объем водорода и один объем хлора дают два объема хлорида водорода. Все это вполне допустимо, если, как указывалось выше, частицы различных газов независимо от того, состоят ли они из одиночных атомов или из комбинаций атомов, равно удалены друг от друга и если расстояние между ними достаточно велико. В этом случае равное число частиц газа (при данной температуре) занимает равные объемы независимо от вида газа. Первым, кто обратил внимание на необходимость предположения о том, что в газах равное число частиц занимает равные объемы, был итальянский химик Амедео Авогадро (1776—1856). Поэтому предположение, выдвинутое им в 1811 г., получило название гипотезы Авогадро. Если твердо помнить эту гипотезу, то можно провести четкое различие между атомами и молекулами водорода (пары атомов), а также между атомами и молекулами других газов. Тем не менее еще в течение полувека после смерти Авогадро химики пренебрегали этой гипотезой и не проводили различия между атомами и молекулами важнейших газообразных элементов. Неопределенность наблюдалась и при определении атомных весов некоторых наиболее важных элементов. К счастью, установить правильные атомные веса можно и другими способами. Например, в 1818 г. французский химик Пьер Лун Дюлонг (1785—1838) и французский физик Алексис Терез Пти (1791—1820) определили атомный вес одного из таких элементов [42]. Они обнаружили, что удельная теплоемкость элементов (количество теплоты, которое необходимо подвести к единице массы вещества, чтобы повысить его температуру на один градус) обратно пропорциональна атомному весу. Иными словами, если атомный вес элемента x вдвое больше атомного веса элемента у, то после поглощения одинаковыми весовыми количествами элементов одинакового количества тепла температура у повысится вдвое больше, чем температура x. Это и есть закон удельных теплоемкостей. Таким образом, атомный вес элемента (правда, только приблизительный) можно определить, измерив его теплоемкость. Этот метод оказался пригодным только для твердых элементов, да и то не для всех, и тем не менее это был шаг вперед. Немецкий химик Эйльгард Митчерлих (1794—1863) в 1819 г. нашел, что соединения, имеющие сходный химический состав, обычно выделяются в виде смешанных кристаллов, как будто молекулы одного вещества перемешиваются с аналогичными по форме молекулами другого вещества. Таким образом был постулирован закон изоморфизма («одинаковой формы»). Из этого закона следует, что если два аналогичных по составу соединения кристаллизуются в виде смешанных кристаллов, то их химическую природу можно считать подобной (изоморфной). Это свойство изоморфных кристаллов позволяло экспериментаторам делать правильные заключения об атомных весах молекул одинакового элементного состава. Веса и символы Поворотный этап в истории развития химической атомистики связан с именем шведского химика Иёнса Якоба Берцелиуса [43]. Он вслед за Дальтоном внес особенно большой вклад в создание атомистической теории. Примерно о 1807 г. Берцелиус вплотную занялся определением точного элементного состава различных соединений. Проведя не одну сотню анализов, он представил столько доказательств, подтверждавших закон постоянства состава, что химики были вынуждены признать справедливость этого закона, а следовательно, и принять атомистическую теорию, которая непосредственно вытекала из закона постоянства состава. Далее Берцелиус принялся за определение атомных весов более сложными и точными методами, которые были недоступны Дальтону. В этой своей работе Берцелиус использовал законы, открытые Дюлонгом и Пти, Митчерлихом и Гей-Люссаком (но, подобно большинству своих современников, не воспользовался гипотезой Авогадро). В 1826 г. Берцелиус опубликовал первую таблицу атомных весов. Приведенные в ней величины в основном совпадают (за исключением атомных весов двух-трех элементов) с принятыми в настоящее время. Эта таблица, опубликованная в издававшихся самим И. Берцелиусом «Годичных обзорах», вошла в историю химии как таблица 1826 г. Существенное различие между таблицами Берцелиуса и Дальтона состоит в том, что величины, полученные Берцелиусом, в большинстве не были целыми числами. В своих расчетах Дальтон исходил из того, что атомный вес водорода равен 1, и поэтому атомные веса всех элементов в таблице Дальтона представляют собой целые числа. Изучив составленную Дальтоном таблицу атомных весов, английский химик Уильям Праут (1785—1850) пришел в 1815—1816 гг. к мнению, что все элементы в конечном счете состоят из водорода и что атомные веса различных элементов различаются по той причине, что они состоят из разного числа атомов водорода. Эта точка зрения известна как гипотеза Праута. Однако таблица Берцелиуса, казалось, разрушила это привлекательное предположение (привлекательное потому, что, подобно античным ученым, Праут сводил все возраставшее число элементов к одному основному веществу и, таким образом, как будто бы придавал Вселенной упорядоченность и симметрию). Однако, если принять атомный вес водорода («основы»), равным 1, то атомный вес кислорода составит приблизительно 15.9 веса водорода, но едва ли можно согласиться с тем, что кислород состоит из 15 плюс еще 9/10 атома водорода. В следующем столетии таблицы атомных весов постоянно уточнялись, и все более очевидными становились выводы Берцелиуса, считавшего, что атомные веса различных элементов не являются целыми числами, кратными атомному весу водорода. В шестидесятых годах XIX в. бельгийский химик Жан Сервэ Стас (1813—1891) определил атомные веса точнее, чем Берцелиус. В начале XX в. американский химик Теодор Уильям Ричардс (1868—1928), приняв все меры предосторожности (во многом надуманные), определил величины атомных весов с такой точностью, которая только возможна при использовании чисто химических методов. Исследования Стаса и Ричардса ответили на те вопросы, которые в работах Берцелиуса оставались нерешенными. Нельзя было не принять тот факт, что атомные веса выражаются нецелыми числами, и в свете этого гипотеза Праута, казалась бы, все более теряла смысл. Однако в то время, когда Ричарде проводил свои поразительно точные определения атомных весов, вновь встал вопрос о том, что следует понимать под атомным весом. И на этом этапе развития химии гипотезе Праута, как мы увидим далее, суждено было возродиться. 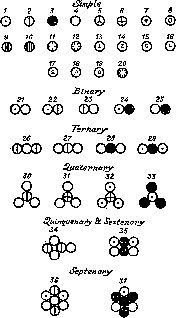 Рис. 9. Символы некоторых элементов и соединений, предложенные Дальтоном; 1 — водород; 3 — углерод; 4 — кислород; 15 — медь; 17 — серебро; 19 — золото; 21 — вода. Дальтон дал неверную формулу воды (НО вместо Н2О), но его формулы монооксида (25) и диоксида углерода (28) верны. Поскольку, как выяснилось, атомные веса различных элементов взаимосвязаны не столь простым образом, как это ранее предполагалось, необходимо было выявить стандарт, исходя из которого можно было бы определять атомные веса элементов. Естественным казалось принять за единицу атомного веса атомный вес водорода, как это сделали Берцелиус и Дальтон. Но при этом атомный вес кислорода выражался неудобным нецелым числом 15.9, а ведь именно кислород обычно использовался для определения соотношений элементов в различных соединениях. Чтобы атомный вес кислорода выражался удобным целым числом при минимальном нарушении стандарта, т. е. атомного веса водорода, атомный вес кислорода округлили и приняли равным 16.000 (вместо 15.9). Таким образом, в качестве стандарта был принят атомный вес кислорода, равный 16; атомный вес водорода при этом оказался равным 1.008. Атомный вес кислорода служил стандартом вплоть до середины XX в. После того как атомистическая теория была принята, стало возможным изображать вещества в виде молекул, содержащих постоянное число атомов различных элементов. Вполне естественным было попытаться изобразить такие молекулы в виде набора маленьких кружков, представляющих собой атомы; при этом атомы каждого вида можно было изобразить кружками определенного типа. Дальтон пытался ввести именно эту символику. Простым кружком он изображал атом кислорода; кружком с точкой посередине — атом водорода; кружком с вертикальной линией — атом азота; закрашенным черным кружком — атом углерода и т. д. Поскольку придумывать различные типы кружков становилось все труднее и труднее, Дальтон стал использовать начальные буквы названий элементов. Так, серу он изображал в виде кружка с буквой S, фосфор — в виде кружка с буквой P и т. д. Берцелиус решил, что кружки излишни, достаточно лишь начальных букв. Он предложил, чтобы каждому элементу соответствовал свой особый знак, который был бы одновременно и символом элемента, и символом одиночного атома этого элемента, и в качестве такого знака предложил использовать начальную букву латинского названия элемента. (К счастью, для англоязычных народов латинское название почти всегда похоже на английское.) В тех случаях, когда названия двух или более элементов начинались с одних и тех же начальных букв, добавлялась вторая буква названия. Так появились химические символы элементов, которыми пользуются во всем мире и поныне. Итак, химическим символом углерода, водорода, кислорода, азота, фосфора и серы стали соответственно C, H, O, N, P и S, кальций и хлор (углерод первым завладел прописной буквой C) обозначались соответственно Ca и Cl. С помощью химических символов легко показать количество атомов в молекуле. Так, молекулу водорода, состоящую из двух атомов водорода, записывают как H2, а молекулу воды, содержащую два атома водорода и один атом кислорода,— как H2O. (Знак без числового индекса, это легко увидеть, означает единичный атом.) Углекислый газ — это CO2, серная кислота — H2SO4, а хлорид водорода — HCl. Химические формулы этих простых соединений говорят сами за себя. Химические формулы можно объединять в химические уравнения, описывающие реакции. С помощью такого уравнения можно, например, показать, что углерод соединяется с кислородом и образует углекислый газ: C + O2 > CO2. В таких уравнениях, чтобы не нарушить закона сохранения массы веществ, необходимо учитывать все участвующие в реакции атомы. Предположим, мы хотим сказать, что водород соединяется с хлором и образует хлорид водорода. Если это записать просто как H2 + Cl2 > HCl, то нетрудно заметить, что среди исходных веществ у нас два атома водорода и два атома хлора, а среди продуктов реакции — только по одному. Чтобы уравнять правую и левую части, перед формулами исходных веществ и продуктов реакции ставят коэффициенты. В результате реакция образования хлорида водорода записывается как H2 + Cl2 > 2HCl, а реакция образования воды — как 2H2 + O2 > 2H2O. Электролиз Изучая влияние электрического тока на химические вещества, ученые смогли выделить ряд новых элементов. Вообще за полтора века, прошедшие с того времени, когда Бойль ввел понятие «элемент» (см. гл. 3), было открыто поразительно много веществ, отвечающих этому определению. Более того, было установлено, что некоторые простые и сложные вещества содержат неоткрытые элементы, которые химики не могли пока ни выделить, ни изучить. Очень часто эти элементы входили в состав оксидов, т. е. соединений кислорода. Чтобы выделить элемент, соединенный с кислородом, последний необходимо было удалить. В принципе под воздействием какого-либо другого элемента, обладающего более сильным сродством к кислороду, атом (или атомы) кислорода может покинуть первый элемент и присоединиться ко второму. Этот метод оказался эффективным. Причем часто роль второго, отнимающего кислород, элемента выполнял углерод. Например, если железную руду, которая по сути является оксидом железа, нагревать на коксе (относительно чистая разновидность углерода), то углерод соединяется с кислородом; при этом образуются оксиды углерода и металлическое железо. Рассмотрим теперь известь. По своим свойствам она тоже похожа на оксид. Однако ни один из известных тогда элементов, вступая в реакцию с кислородом, не образует известь. Следовательно, известь является оксидом неизвестного элемента. Пытаясь выделить этот неизвестный элемент, известь нагревали на коксе, но при этом ничего не происходило. Неизвестный элемент, по-видимому, так крепко удерживал кислород, что атомы углерода не могли оторвать от него атомы кислорода. Ни одно другое химическое вещество также не могло «заставить» известь отдать кислород. Однако английский химик Гемфри Дэви (1778—1829) решил, что если вещество нельзя разложить химическим путем, то, возможно, это удастся осуществить под воздействием электрического тока: ведь таким способом удалось разложить даже молекулу воды. Дэви сконструировал электрическую батарею, в которой насчитывалось более 250 металлических пластин; это была самая сильная из имевшихся в то время батарей. Пропуская ток, который давала эта батарея, через растворы соединений, предположительно содержащих неизвестные элементы, Дэви пытался таким образом выделить эти элементы, однако успеха не добился. Он только разложил воду и получил водород и кислород. Очевидно, необходимо было прежде удалить воду. Однако через твердые вещества ему даже не удалось пропустить ток. Наконец, Дэви догадался расплавить соединения и пропустить ток через расплав. Это оказалось действенным. 6 октября 1807 г. Дэви пропустил ток через расплавленный поташ (карбонат калия) и получил маленькие шарики металла, который он назвал потассием (от английского — potash). Этот металл, впоследствии названный калием, оказался очень активным. Он вытеснял кислород из воды, освобождая водород, причем реакция эта шла чрезвычайно бурно. Неделю спустя Дэви выделил из соды (карбоната натрия) содий (от английского — soda), впоследствии названный натрием. По своей активности, как выяснилось, натрий лишь незначительно уступает калию. В 1808 г., пользуясь модифицированным вариантом метода Берцелиуса, Дэви выделил несколько металлов из их оксидов: магний из магнезии, стронций из оксида стронция, барий из оксида бария и кальций из извести («кальций» — от латинских названий извести — calx, calcis). Дэви также показал, что зеленоватый газ, который открывший его Шееле (см. гл. 4) считал оксидом, в действительности является элементом. Дэви предложил назвать его хлорин (от греческого ?????? — желто-зеленый). Позднее Гей-Люссак сократил это название до хлора. Дэви доказал, что соляная кислота, будучи сильной кислотой, не содержит атома кислорода в своей молекуле, и, таким образом, опроверг предположение Лавуазье, который рассматривал кислород как необходимый компонент всех кислот (см. гл. 4.) Работы Дэви по электролизу продолжил его помощник и ученик Майкл Фарадей (1791—1867) [44], который впоследствии стал знаменитым ученым. Ряд электрохимических терминов, введенных Фарадеем, используется и по сей день (рис. 10). Так, например, он назвал расщепление молекул под действием электрического тока электролизом. По предложению специалиста по античной филологии Уильяма Уэвелла (1794—1866) Фарадей назвал соединение или раствор, способный проводить электрический ток, электролитом; металлические стержни или пластины, помещенные в расплавленный металл или раствор,— электродами; электрод, несущий положительный заряд,— анодом; электрод, несущий отрицательный заряд,— катодом. 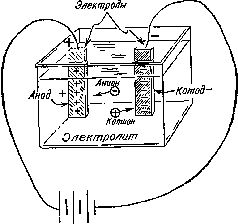 Рис. 10. Электролитический процесс Фарадей объяснял с помощью следующей схемы. Обозначения на рисунке соответствуют предложенной им терминологии. Реально существующие частицы, благодаря которым электрический ток проходит через раствор или расплав, Фарадей назвал ионами (от греческого ??? — идущий). Ионы, перемещающиеся по направлению к аноду, он назвал анионами, а ионы, перемещающиеся по направлению к катоду,— катионами. В 1832 г. Фарадей установил, что электрохимические процессы характеризуются определенными количественными соотношениями, и сформулировал следующие два закона электролиза. Вес вещества, выделившегося на электроде во время электролиза, пропорционален количеству электричества, пропущенного через раствор. Вес металла, выделенного данным количеством электричества, пропорционален эквивалентному весу этого металла. Таким образом, если при взаимодействии серебра и калия с заданным количеством кислорода серебра в 2.7 раза больше, чем калия, то при данном количестве электричества серебра выделится в 2.7 раза больше, чем калия. Законы Фарадея, по мнению некоторых химиков, указывали на то, что электричество, как и материю, можно разложить на постоянные минимальные единицы, или, другими словами, на «атомы электричества». Предположим, что при пропускании электричества через раствор атомы материи притягиваются к катоду или к аноду «атомами электричества», и предположим, что для управления одним «атомом материи» во многих случаях достаточно одного «атома электричества», но иногда требуются два или даже три «атома электричества». Представив себе это, легко объяснить законы электролиза Фарадея. Однако справедливость этого предположения была подтверждена только в самом конце XIX в., и тогда же было введено понятие «атомы электричества». Сам Фарадей никогда не проявлял энтузиазма по поводу «атомов электричества», да и атомистического учения в целом. [45] Примечания:[3] Железо земного (не метеоритного) происхождения было известно народам Южного Кавказа уже в 2100 г. до н. э. [4] О процессе формирования представлений об «элементах-стихиях» см.: Ахутин А. В. Мифологические истоки учения об элементах. В кн.: Всеобщая история химии. Возникновение и развитие химии с древнейших времен до XVII в.— М.: Наука, 1980, с. 74—91. [35] История формирования представлений о химическом соединении рассмотрена в кн.: Шептунова З. И. Химическое соединение и химический индивид (очерк развития представлений).— М.: Наука, 1972, 212 с. [36] Термин стехиометрия (от греческого ????????? — стихия, начало, элемент, основа) был введен И. Рихтером для обозначения соотношения масс кислот и оснований при образовании солей.— Прим. перев. [37] В действительности состав некоторых соединений может колебаться в определенных пределах, но это особые случаи. Состав тех простых соединений, которыми занимались химики до 1800 г., строго соответствует требованиям закона постоянства состава. [38] См.: Дальтон Дж. Сборник избранных работ по атомистике. Под ред. и с примечаниями Б. М. Кедрова.— М.: Госхимиздат, 1940, 244 с; Кедров Б. М. Атомистика Дальтона.— М.-Л.: Госхимиздат, 1949, 312 с. [39] Столетие спустя это представление претерпело изменение. В конце концов один атом можно превратить в другой (см. гл. 14). Однако достичь этого можно, лишь пользуясь такими методами, которых не мог бы себе ни представить, ни осуществить ни один алхимик. [40] Атомный вес — это не вес как сила и вовсе не масса, а число, выражающее отношение главным образом масс атомных ядер. Процесс взвешивания, имевший место при определении атомных весов, был процессом сравнения масс.— Прим. ред. [41] См.: Быков Г. В. Амедео Авогадро, Очерк жизни и деятельности.— М.: Наука, 1970, 184 с. [42] Работа Дюлонга и Пти была опубликована в 1819 г.— Прим. перев. [43] См.: Соловьев Ю. И., Куринной В. И. Якоб Берцелиус. Жизнь и деятельность.— М.: Наука, 1980, 2-е изд., 320 с. [44] См.: Кудрявцев П. С. Фарадей.— М.: Просвещение, 1969, 168 с. [45] См.: Крицман В. А. Роберт Бойль. Джон Дальтон. Амедео Авогадро. Создатели атомно-молекулярного учения в химии.— М.: Просвещение, 1978, 144 с. |
|
|||
|
Главная | В избранное | Наш E-MAIL | Добавить материал | Нашёл ошибку | Наверх |
||||
|
|
||||
