|
||||
|
Глава 11 Неорганическая химия Новая металлургия Хотя читателю может показаться, что XIX в., особенно его вторая половина, был веком органической химии, неорганическая химия в этот период также продолжала развиваться. Одним из достижений в этой области явилось изобретение фотографии (см. гл. 9). Однако на развитии экономики или благосостоянии общества это изобретение, естественно, практически не сказалось. Еще одним достижением неорганической химии явилось усовершенствование способа зажигания огня. На протяжении тысячелетий человек добывал огонь трением. Со времени появления железа он научился высекать искры, ударяя огнивом (кресалом) о кремень. Оба способа были неудобны и утомительны, и со временем люди начали пытаться использовать для получения огня химические вещества, способные загораться при низких температурах в результате кратковременного трения. В 1827 г. английский изобретатель Джон Уолкер (приблизительно 1781—1859 гг.) предложил первые вполне пригодные для употребления фосфорные спички. За последующие полтора столетия спички значительно усовершенствовались, однако принцип их действия остался тем же. Фотография и фосфорные спички — только два примера практических успехов неорганической химии. В полных и подробных трудах по истории химической науки эти и подобные им примеры заслуживают более чем простого упоминания, но в нашей краткой работе мы должны сосредоточить свое внимание на открытиях более крупных. Самые большие успехи в области прикладной неорганической химии, безусловно, связаны с получением металлов и прежде всего стали, производство которой было и остается наиболее важной статьей экономики любой промышленно развитой страны. Если нефть для современного общества — источник сырья и топлива, то сталь — материальная основа практически всех отраслей промышленности. Сталь, как мы отметили, начали получать и широко использовать еще три тысячелетия назад, но только в середине XIX в. был разработан способ, который обеспечивал массовое производство литой стали. Большая заслуга в этом принадлежит английскому металлургу Генри Бессемеру (1813—1898). Бессемер работал над созданием артиллерийского снаряда, который вращался бы в полете и двигался по точно заданной траектории. Для этого Бессемеру необходимо было орудие с нарезным стволом, т. е. такое орудие, в стенках канала ствола которого имелись бы спиральные канавки, прорезанные от заднего конца ствола до дульного среза. Такое орудие можно было изготовить только из особо прочной стали, так как ствол его должен был выдерживать высокие давления, необходимые для вжимания выступов снаряда в спиральные канавки. Использовавшиеся в то время обычные орудия с ненарезным стволом можно было изготавливать из менее прочного металла. Производство стали обходилось весьма дорого, и пока такое положение дел сохранялось, едва ли кто-нибудь согласился выпускать орудия нового типа. Процесс получения железа начинается со стадии выплавки чугуна, содержащего значительное количество углерода (который попадает в чугун из кокса или древесного угля, используемых для плавления руды). Чугун отличается очень большой твердостью, но он хрупок. Из чугуна можно полностью удалить углерод. Образующееся в результате этой операции сварочное железо представляет собой ковкий, но относительно мягкий материал. В него вновь вводят некоторое количество углерода и в результате получают сталь, которая обладает достаточной вязкостью и в то же время достаточной твердостью. Бессемер начал искать такой способ производства стали, который позволил бы исключить дорогостоящую стадию получения сварочного железа. Чтобы удалить избыточный углерод из чугуна, он пропускал через расплавленный металл струю воздуха. Металл при этом не охлаждался и не затвердевал; наоборот, в результате реакции углерода с кислородом выделялось тепло, и температура расплава повышалась. Прекращая в соответствующий момент подачу воздуха, Бессемер смог получить сталь (рис. 19). 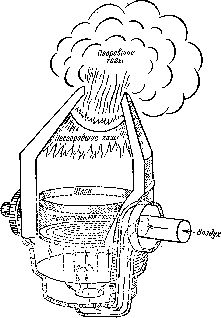 Рис. 19. Схема конвертера Бессемера. С изобретением конвертера технология производства стали полностью изменилась. В 1856 г. Бессемер опубликовал сообщение об изобретенном им конвертере. Первые попытки повторить опыты Бессемера окончились неудачей: получить таким методом сталь можно было только из руды, не содержащей фосфора. Как только это удалось установить, дело пошло на лад. В результате сталь стала дешевой, и железный век (см. гл. 1) уступил дорогу веку стальному. (В последующие годы технология производства стали значительно усовершенствовалась; были разработаны новые способы, превосходящие способ Бессемера.) Значение стали трудно переоценить. Сталь — это современные небоскребы и подвесные мосты, сталь — это рельсы для поездов, сталь — это мощные боевые корабли и всесокрушающая артиллерия. Однако сколь совершенным материалом ни представлялась сталь, металлурги пытались улучшить ее свойства, и в результате список компонентов, входящих в состав стали, значительно расширился. Английский металлург Роберт Эббот Хэдфилд (1858—1940) изучал влияние на свойства стали добавок других металлов. Хэдфилд знал, что добавка марганца делает сталь хрупкой, но он решил ввести в сталь марганца больше, чем обычно вводили другие металлурги. Когда содержание марганца достигло 12%, сталь перестала быть хрупкой. Более того, если такую сталь нагреть до 1000°С, а затем охладить в воде, то она станет намного тверже, чем исходный металл. Хэдфилд запатентовал марганцевую сталь в 1882 г., и с этого момента началось победное шествие легированных сталей. Добавляя в сталь хром, молибден, ванадий, вольфрам и ниобий, металлурги получили богатый спектр легированных сталей, обладающих самыми различными свойствами. К 1919 г. американский изобретатель Элвуд Хэйнес (1857—1925) запатентовал нержавеющую сталь, содержащую в качестве добавок хром и никель. В 1916 г. японский металлург Котаро Хонда (1870—1954) обнаружил, что магниты, изготовленные из вольфрамовой стали, к которой добавлен кобальт, отличаются большей мощностью, чем магниты из обычной стали. Это открытие проложило путь к разработке еще более сильных магнитных сплавов. В это же время начали находить применение и новые металлы, в частности алюминий. Содержание этого металла в земной коре выше, чем содержание железа; более того, алюминий — самый распространенный металл. Однако в природных соединениях он прочно связан с другими элементами. В то время как железо было известно и добывалось из руды еще в доисторические века, алюминий (см. гл. 6) даже не считался металлом, пока Вёлер не выделил в 1827 г. не вполне чистый образец алюминия. Лишь в 1855 г. французский химик Анри Этьен Сен-Клер Девилль (1818—1881) разработал приемлемый способ получения достаточных количеств довольно чистого алюминия. Однако и после этого стоимость его намного превышала стоимость стали; так, достаточно сказать, что из алюминия были сделаны такие «престижные» предметы, как погремушка сыну Наполеона III и головной убор статуи Вашингтона. В 1886 г. молодой американский студент-химик Чарльз Мартин Холл (1863—1914), услышав от своего учителя, что тот, кто откроет дешевый способ получения алюминия, несомненно, разбогатеет и прославится, решил заняться этой проблемой. Работая в домашней лаборатории, он открыл, что оксид алюминия (глинозем) можно растворить в расплавленном минерале криолите. А получив раствор оксида, можно путем электролиза выделить и сам алюминий. В том же году французский металлург Поль Луи Туссен Эру (1863—1914) разработал по сути тот же метод получения алюминия. Метод Холла — Эру сделал алюминий настолько дешевым, что из него стали изготавливать даже кухонную посуду. Наиболее ценное свойство алюминия — его легкость (алюминий в 3 раза легче стали). Именно по этой причине он так широко используется в авиационной промышленности. В этих же целях потребляются и большие количества магния — еще более легкого металла. В 30-х годах были разработаны практически осуществимые методы извлечения магния из его солей, растворенных в морской воде, так что на сегодняшний день мы располагаем поистине неистощимым источником этого металла. (В настоящее время из морской воды получают и бром, и йод, и, конечно же, поваренную соль. Важной задачей, значение которой в будущем еще более возрастет, является получение пресной воды из океана.) Многообещающими представляются также металлы, подобные титану. Титан — достаточно распространенный металл, отличается высокой устойчивостью к действию кислот; он легче стали, но тяжелее алюминия. Обработанный соответствующим образом, титан является самым прочным из металлов с примерно такой же удельной массой. Цирконий похож по свойствам на титан, но он менее распространен и тяжелее титана. Перспективы использования титана весьма велики, особенно в связи с созданием сверхзвуковых самолетов. Самолеты, летающие со скоростью, в несколько раз превышающей скорость звука, даже в верхних разреженных слоях атмосферы испытывают значительное сопротивление вследствие трения воздуха. Их наружная обшивка должна выдерживать высокие температуры, и в качестве материала для такой обшивки особенно подходит титан, так как по сравнению с другими металлами он сохраняет высокую прочность при повышенных температурах. Азот и фтор Азот — основной компонент воздуха, на его долю приходится 78% всего объема. Большинство организмов используют его только в виде соединений, а содержащийся в воздухе молекулярный азот практически инертен и с трудом вступает в реакции. Хотя воздух есть повсюду, в почве часто ощущается недостаток нитратов (наиболее распространенного типа соединений азота), который приходится восполнять, внося в почву органические или минеральные удобрения. Соединения азота расходуются в огромных количествах: они используются в производстве минеральных удобрений, взрывчатых веществ и порохов, красителей и полупродуктов органического синтеза. Опасаясь нехватки природного сырья, химики начали изучать возможность использования азота воздуха. Этим вопросом занимался, в частности, немецкий химик Фриц Габер (1868—1934). Он выяснил, что азот вступает в реакцию с водородом при высоком давлении и высокой температуре в присутствии катализатора (железа), и поставил себе целью найти способ получения аммиака из азота воздуха и водорода. Превратить аммиак в нитраты было несложно. К 1908 г. Габер решил эту задачу. Почти сразу же после начала первой мировой войны британский флот блокировал Германию, в результате чего в эту страну перестал поступать нитрат из Чили (наилучшее природное сырье). Между тем он был необходим для ведения войны, и вот немецкий химик Карл Бош (1874—1940) начинает работать над реакцией Габера, пытаясь создать промышленный способ получения аммиака, и к середине войны в Германии уже было налажено промышленное производство соединений азота. [106] Совсем иначе обстояло дело с фтором. Этот элемент настолько активен, что существует только в виде соединений, поэтому попытки выделить его в свободном состоянии не приводили к успеху. И тем не менее еще со времен Лавуазье химики были уверены в существовании этого элемента. Так, Ньюлендс и Менделеев включили фтор в свои периодические таблицы (см. гл. 8), хотя к тому времени этот газ еще никто не получил. Конечно, при электролизе фтор отщепляется от содержащей его молекулы, однако в элементной форме он настолько активен, что сразу же вступает в реакцию и опять становится частью какого-то соединения. (Фтор — самый активный из всех химических элементов.) В XIX в. проблемой получения фтора занимались многие химики, начиная с Гемфри Дэви. Успех выпал на долю французского химика Анри Муассана (1852—1907). Муассан решил, что поскольку платина относится к числу тех немногих веществ, на которые фтор не действует, то не остается ничего другого, как изготовить, несмотря на дороговизну, все оборудование из платины. Более того, чтобы понизить активность фтора, он охладил реакционную смесь до -50°С. Поместив раствор фторида калия в плавиковой кислоте в специально изготовленный платиновый сосуд, Муассан пропустил через раствор электрический ток и достиг цели. Так в 1886 г. был наконец выделен бледно-желтый газ — фтор. Однако шумную известность Муассану принесло не получение фтора, а совсем другая работа, которая, как выяснилось позднее, в сущности ни к чему не привела. Древесный уголь и алмаз являются разновидностями углерода; алмаз отличается от угля только более плотной упаковкой атомов. Следовательно, под действием высокого давления атомы в кристалле древесного угля могут перегруппироваться и образовать алмаз. И Муассан попытался получить таким образом драгоценный камень. Он растворил древесный уголь в расплавленном железе и вылил полученную массу в воду, считая, что при резком охлаждении углерод будет кристаллизоваться в виде алмаза. Примерно в 1893 г. Муассан получил несколько мельчайших кристалликов черного цвета, которые он счел алмазами, и кристаллик хорошего алмаза длиной более 0.5 мм. Казалось бы, Муассан достиг успеха. Однако ни он сам, ни его последователи не смогли повторить этот опыт. Как мы теперь знаем, в таких условиях алмаз образоваться не мог; скорее всего Муассан стал жертвой мистификации: кто-то из его ассистентов подбросил алмазы в железо. Американский изобретатель Эдвард Гудрич Ачесон (1856—1931) также пытался получить алмаз из более обычных форм углерода. Он не достиг цели, но, нагревая углерод в присутствии глины при высоких температурах, получил чрезвычайно твердый карбид кремния, названный им карборундом. Полученное вещество оказалось превосходным абразивным материалом. Для получения алмазов необходимы сверхвысокие давления, которые не были доступны в XIX в. Высокие давления в сочетании с высокими температурами позволяют атомам более или менее легко менять свои положения. Под действием высоких давлений различные элементы и соединения принимают новые формы, в которых атомы и молекулы упакованы необычайно плотно. Например, лед. становится значительно более плотным, чем вода, а температура его плавления превышает температуру кипения воды при обычных давлениях [107]. И в 1955 г. по методу Бриджмена были получены наконец первые синтетические алмазы. На границе органической и неорганической химии В XX в. начала приоткрываться завеса над обширной областью, прилегающей к границе органической и неорганической химии [108]. В 1899 г. английский химик Фредерик Стенли Киппинг (1863—1949) занялся изучением органических соединений, содержащих кремний — самый распространенный после кислорода элемент земной коры. Киппинг посвятил изучению кремния более сорока лет и синтезировал множество органических соединений, содержащих один или несколько атомов кремния. Как выяснилось, можно получать бесконечно длинные цепи, состоящие из чередующихся атомов кремния и кислорода. Поскольку валентность кремния равна четырем, а в образовании связей с кислородом участвуют лишь две связи, две другие связи кремния в такой цепи остаются свободными, и к нему могут присоединяться различные органические группы. Во время второй мировой войны и особенно после окончания войны сильно возросло значение таких элементоорганических соединений, как силиконы, используемых в качестве смазок, гидравлических жидкостей, синтетических смол, водоотталкивающих средств и т. д. Обычные органические соединения состоят из атомов углерода, к которым присоединены другие атомы. Как правило, «другие атомы» — это атомы водорода, поэтому об органических соединениях можно говорить как об углеводородах и их производных. Однако известно, что атом фтора почти столь же мал, как и атом водорода. В связи с этим резонно было предположить, что там, где подходит атом водорода, подойдет и атом фтора, т. е. наряду с семейством углеводородов существует семейство фторуглеродов и их производных. Первые эксперименты с фторорганическими соединениями провел американский химик Томас Мидгли-младший (1889—1944). В 1930 г. он получил фреон, молекула которого состоит из атома углерода и присоединенных к нему двух атомов хлора и двух атомов фтора. Фреон легко сжижается, следовательно, его можно использовать в качестве холодильного агента вместо таких легко сжижаемых газов, как аммиак и диоксид серы. В отличие от этих газов фреон не имеет запаха, нетоксичен и не воспламеняется. В настоящее время фреон почти повсеместно применяется в домашних холодильниках и кондиционерах. Во время второй мировой войны фтор и его соединения использовались в работах, связанных с ураном и атомной бомбой (см. гл. 14). В ходе работ потребовались такие смазочные вещества, которые выдерживали бы действие фтора. В качестве таковых были выбраны фторуглероды, поскольку они, так сказать, уже выдержали воздействие фтора. Фтор образует очень прочные связи с углеродом, и фторуглеродные цепи более стабильны и инертны, чем углеводородные. Фторуглеродные полимеры представляют собой воскообразные, водоотталкивающие, устойчивые к действию растворителей вещества, обладающие электроизоляционными свойствами. В 60-х годах из фторуглеродной пластмассы тефлона начали изготавливать (покрывать изнутри) сковороды. На таких сковородах, например, можно жарить без масла и продукт не пригорает. Некоторые неорганические комплексы образуются вообще без участия атомов углерода. В 1909 г. немецкий химик Альфред Шток (1876—1946) начал изучать гидриды бора — соединения бора и водорода и установил, что соединения этого ряда могут быть довольно сложными и до некоторой степени похожими на углеводороды. После окончания второй мировой войны гидриды бора неожиданно нашли применение в качестве добавок к ракетным топливам для повышения силы тяги, движущей ракету в верхних слоях атмосферы и в космическом пространстве. Кроме того, началось интенсивное изучение гидридов бора, поскольку обычные формулы, подобные предложенным Кекуле (см. гл. 6), не позволяли объяснить их строение. Тем не менее все перечисленные успехи, достигнутые в результате большой изобретательности и настойчивости ученых, оказались в стороне от наиболее важных направлений химии XX в. Ученые, посвятившие себя теоретической химии, пытались «заглянуть» за оболочку атома. Чтобы узнать, что же они там нашли, нам придется в оставшихся главах книги вернуться к основной линии развития истории химии [109]. Примечания:[1] А. Азимов связывает накопление химических знаний прежде всего с появлением и развитием металлургии. Однако ремесленная химия древности была гораздо шире. Параллельно с металлургией развивалась техника изготовления красок (минеральных и растительных) и крашения, изготовления стекла и керамики. Наряду с металлургией важной основой дальнейшего развития экспериментальной химии была фармация. [10] И в Древнем Риме, и позднее в Византийском государстве накопление химических знаний продолжалось благодаря развитию фармации. Так, «Геопоника», компиляция из 20 книг, приписываемая Кассину Бассу (VII в.), содержала массу практических рецептов и мистические толкования химических процессов. [106] Биографии великих химиков. Пер. с нем./Под ред. Г В. Быкова, С. А. Погодина.— М.: Мир, 1981. [107] При снятии давления такие вещества, как правило, возвращаются в обычное состояние. Алмаз составляет исключение. [108] А. Азимов лишь очень кратко касается развития одной из важнейших и в познавательном, и практическом смысле областей химии — химии элементоорганических соединений. Не упоминает он и о работах Виктора Гриньяра (1871 — 1935), получившего в 1900 г. магний-галогенорганические соединения (реактивы Гриньяра). Вклад советских ученых П. П. Шорыгина, А. Е. Арбузова, А. Н. Несмеянова, К. А. Кочешкова, К. А. Андрианова в развитие элементоорганической химии особенно велик. Достаточно упомянуть о синтезе кремнийорганических соединений, проведенном К. А. Андриановым, уже в 30-х годах запатентовавшим свои открытия. Не упоминает А. Азимов и об открытии органических соединений переходных металлов. Вместе с тем синтез ферроцена, дибензилхрома был своеобразной химической сенсацией и стимулировал многочисленные теоретические и экспериментальные исследования. См.: Соловьев Ю. И., Трифонов Д. Н., Шамин А. Н. История химии (примечание 13 к гл. 10). [109] По материалам этой главы см.: Развитие органической химии в СССР. (Серия «Советская наука и техника за 50 лет»).— М.: Наука, 1967, 575 с. |
|
|||
|
Главная | В избранное | Наш E-MAIL | Добавить материал | Нашёл ошибку | Наверх |
||||
|
|
||||
