|
||||
|
7. Биллиардные шары как строительный материал Мы знаем, что «строительный материал» кристаллов – атомы имеют очень сложное собственное строение: на различных расстояниях от положительно заряженного ядра, состоящего в свою очередь из ряда более мелких частиц, вращаются электроны, несущие отрицательный заряд[4]. Однако в очень многих случаях – позднее мы скажем, в каких именно, – для воспроизведения расположения атомов в кристалле их можно уподобить шарам. Такое представление об атомах отнюдь не отражает всей их сложной природы, но правильно передаёт одно важное обстоятельство, а именно: рентгеновские исследования структуры кристаллов приводят нас к мысли, что кристаллы строятся по принципу наиболее плотной упаковки шаров. Для того чтобы ясно представить себе сущность этого принципа, возьмём большое количество биллиардных шаров и начнём укладывать их, стремясь создать наиболее плотную упаковку. Прежде всего составим плотный слой – он выглядит так, как биллиардные шары, собранные «треугольником» перед началом игры (рис. 19). 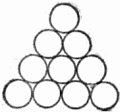 Рис. 19. Один плотный слой шаров. Отметим, что шар внутри треугольника имеет шесть соприкасающихся с ним соседей. Ясно, что нет другого способа составить плотнейший слой из шаров. Будем продолжать укладку наложением слоёв друг на друга. Если бы мы поместили шары следующего слоя непосредственно над шарами первого слоя, то такая упаковка была бы неплотной. Желая разместить в некотором объёме наибольшее число шаров, мы должны положить шары второго слоя в лунки нижележащего. Обратим внимание на то, что заполнить все лунки шарами того же самого размера нельзя: лунки заполняются через одну. Отметим на чертеже чёрным лунки первого слоя, оставшиеся пустыми (рис. 20). Плотная упаковка из двух слоёв также существует лишь одна: мы можем, конечно, заполнить шарами второго слоя все «чёрные» лунки, оставив «белые» пустыми, но от этого вид упаковки не изменится. Однако положение меняется, когда мы переходим к третьему этажу. 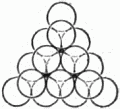 Рис. 20. Два плотных слоя шаров. Чтобы получить плотнейшую упаковку, мы должны укладывать шары третьего слоя в лунки второго. Но при этом шары третьего слоя могут быть размещены двумя способами: либо так, чтобы центры этих шаров лежали над центрами шаров первого слоя, либо так, чтобы их центры лежали над «чёрными» лунками. Наши две трёхэтажные постройки обладают одинаковой плотностью упаковки, но существенно отличаются одна от другой. При наложении 4-го слоя мы ещё более увеличим число возможных упаковок: из двух трёхслойных упаковок мы можем сделать 4 четырёхслойные. Пятислойных будет уже 8 и т.д. Ясно, что число различающихся между собой одинаково плотных шаровых упаковок может быть исключительно велико. Теперь нам надо проследить связь между кристаллической решёткой и шаровой упаковкой. Мы знаем, что основой решётки служат ячейки-кирпичи, прикладыванием которых друг к другу строится кристалл, и какое бы направление мы ни выбрали в кристалле, всегда по этому направлению структура строго повторяется через равные промежутки. А отсюда следует, что кристалл должен представлять собой такую упаковку атомов-шаров, в которой положение слоёв строго повторяется через определённое число слоёв. Если это повторение начинается, например, с 14-го слоя, то это значит, что в высоту ячейка состоит из 13 слоёв. Тогда 14-й слой находится над первым, 15-й – над вторым, 16-й – над третьим и т.д. Самая простая упаковка – двухслойная: третий слой лежит над первым, четвёртый – над вторым и т.д. Это – так называемая гексагональная плотнейшая упаковка. На рисунке 21 показана её решётка (скелет). Кружки и крестики соответствуют положениям центров атомов. Атомы, центры которых обозначены крестиками, входят в лунки как нижнего, так и верхнего слоёв. Этим способом построены, например, кристаллы магния. Исключительно большое распространение имеют трёхслойные кристаллы, в которых 4-й слой повторяет первый, пятый – второй и т.д. Рисунок 22, где по-прежнему отмечены лишь центры атомов, показывает, что в такой упаковке можно выбрать кубическую элементарную ячейку. Плотные слои расположены здесь перпендикулярно диагонали куба, соединяющей два атома, центры которых обозначены кружками. 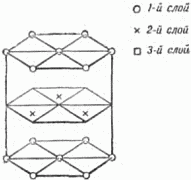 Рис. 21. Скелет плотной гексагональной упаковки. 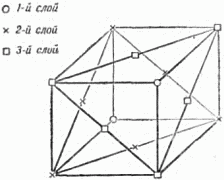 Рис. 22. Скелет гранецентрированной кубической упаковки. (Отмечены центры шаров). Попытайтесь представить себе ячейку расположенной так, чтобы эта диагональ шла вертикально. Левый задний кружок окажется при этом внизу и, единственный на нашем рисунке, будет принадлежать первому слою (центры других атомов этого слоя, принадлежащих соседним ячейкам, на рисунок не попали). На первом слое плотно лежит второй слой: центры шести его атомов, попавших на рисунок, – это крестики, расположенные по вершинам и серединам сторон треугольника. Третий плотный слой представлен шестью квадратиками, расположенными также по треугольнику. Наконец, четвёртый слой, повторяющий первый, содержит на нашем рисунке снова только один кружок. Итак, элементарная ячейка трёхслойной шаровой упаковки – это куб, у которого в вершинах и серединах граней расположены центры атомов. Такую ячейку, называемую кубической гранецентрированной, имеет ряд металлов, например: алюминий, медь, никель, при высокой температуре – железо (о влиянии температуры мы скажем ниже, на страницах 38 и 63). Мы видим теперь, что реальный кристалл представляет собой систему плотно упакованных частиц, расположение которых повторяется в пространстве. Узлы и линии, соединяющие узлы, – лишь мысленная схема, помогающая нам выделить в кристалле элементарный кирпич и наметить направления, в которых его нужно перекладывать, чтобы заполнить весь кристалл. Несколько слов о размерах «шаров»-атомов. Точные измерения, произведённые при помощи рентгеновских лучей, привели к следующим данным: радиусы атомов разных веществ колеблются в небольших пределах, примерно от 0,5 до 2 стомиллионных долей сантиметра. Мы рассматривали упаковки, составленные из одинаковых шаров. Это значит, что пока речь шла о кристаллах химических элементов, содержащих атомы только одного сорта (правда, и элементы не все построены так просто). Перейдём теперь к кристаллам, построенным из атомов нескольких сортов, то есть к кристаллам сложных веществ. |
|
|||
|
Главная | В избранное | Наш E-MAIL | Добавить материал | Нашёл ошибку | Наверх |
||||
|
|
||||
